腫瘤標志物是1978年Herberman在美國國立癌癥研究院召開的人類免疫及腫瘤免疫診斷會上提出的,1979年在英國第七屆腫瘤發生生物學和醫學會議上作為專用術語被大家公認。三十余年來,腫瘤標志物的研究逐漸形成了一門獨立的學科分支。
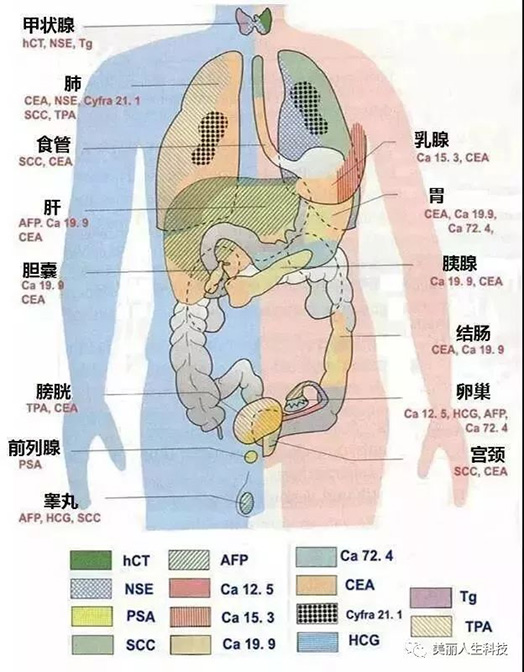
腫瘤標志物,是指在腫瘤發生和增殖過程中,由腫瘤細胞生物合成、釋放或是機體對腫瘤細胞反應而產生的一類物質,這些物質可存在于腫瘤細胞和組織中,也可進入血液和其他體液。當腫瘤發生發展時,這些物質明顯異常,可以利用生物化學、免疫和分子生物學等技術對其進行定性或定量檢測。
腫瘤標志物的血清水平一般與惡性腫瘤的發生、發展、消退、復發等具有良好的相關性,因此測定血清腫瘤標志物水平,可以獲得有關惡性腫瘤的診斷、療效及預后等方面的信息。
1、高危人群的篩查
早期發現、早期診斷、早期治療是腫瘤診治的重要原則。一般認為,利用現代生物物理技術如超聲顯像、計算機X線斷層攝影、磁共振成像等可發現直徑1~1.5cm的腫瘤,而腫瘤生長到2~3mm時即可用免疫學診斷方法測出。腫瘤標志物檢測是發現無癥狀患者的重要線索,可作為腫瘤的輔助診斷工具。
2、腫瘤的鑒別診斷和臨床分期
在臨床已獲得足夠證據證明患者可能患某臟器腫瘤后,腫瘤標志物往往能提供有用的信息幫助區分良、惡性腫瘤和腫瘤類型,如CEA和NSE可輔助區分胃腸道腫瘤是腺癌(CEA陽性、NSE陰性)還是類癌(CEA陰性、NSE陽性);血清腫瘤標志物升高的水平與腫瘤的大小和分化程度有關,其定量檢測有助于輔助診斷臨床分期。
3、腫瘤的復發監測和預后判斷
腫瘤標志物的動態監測有助于判斷腫瘤是否復發。一般建議,治療后第6周進行第一次測定,前3年內每3個月測定1次,3~5年每半年測定一次,5~7年每年一次。如發現腫瘤標志物升高(高于首次值25%),應在2~4周后,再測定1次,連續2次升高者,提示復發或轉移。
腫瘤標志物濃度增加或降低與腫瘤預后密切相關。Newlands等報道HCG和AFP可作為睪丸癌的預后指標,HCG<50U/L的4年生存率為96%,HCG>50U/L或AFP>500U/L的4年生存率為56%。此外,結腸癌時CEA濃度、非霍奇金淋巴瘤時β2微球蛋白濃度、卵巢癌時CA125濃度等的變化都有預后價值。
4、檢測療效
腫瘤標志物有助于明確手術、放療或藥物治療是否有效。通常在成功的治療如腫瘤完全切除和有效化療后,腫瘤標志物即明顯下降,若下降至正常或治療前水平的95%即認為治療成功;如果術后腫瘤標志物未如預期下降,說明手術可能未能成功切除腫瘤。
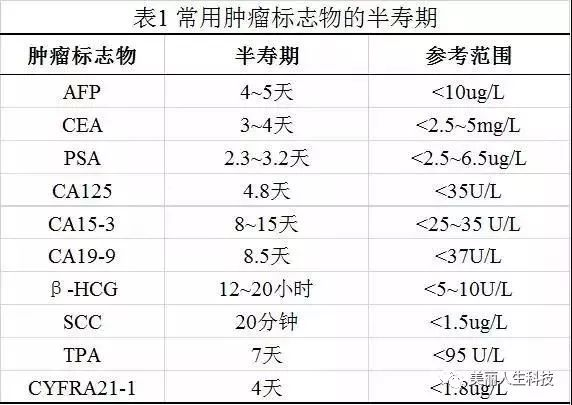
腫瘤標志物下降的時間取決于腫瘤標志物的半壽期,表1是常用腫瘤標志物的半壽期。
5、腫瘤標志物的聯合檢測
一種腫瘤可產生多種腫瘤標志物,不同的腫瘤或同種腫瘤的不同組織類型可有相同的腫瘤標志物,不同的腫瘤患者體內腫瘤標志物的質和量變化也較大。
由于大部分單個腫瘤標志物敏感性或特異性偏低,不能滿足臨床需要,近10年來,理論和實踐上都提倡同時測定多個腫瘤標志物,以提高敏感性和特異性,但聯合檢測的指標必須經科學分析、嚴格篩選,在此前提下,合理選擇3~5項敏感性高、特異性強的腫瘤標志物進行聯合檢測,可避免醫療資源的浪費,減輕患者的經濟負擔。
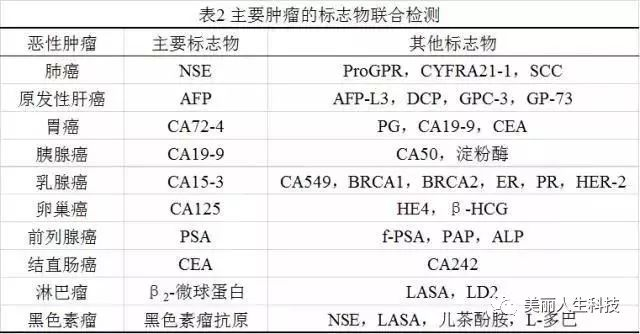
常用腫瘤標志物的組合見表2。
6、腫瘤的個體化醫療
所謂“個體化醫療”,是指在適當的治療時間,使用適當的給藥途徑,對適當的患者施以適當的藥物和適當劑量,以避免不當治療和有害治療,降低藥物的毒副作用。識別患者個體差異的依據主要是某些特定的分子標志物(靶標),實現對這些靶標的準確檢測和評估是腫瘤個體化醫療的基礎。
隨著新靶向藥物的發現及研究的深入,個體化醫療的靶標檢測也將從單一靶標檢測發展為多靶標聯合檢測,最終形成靶標檢測系統,有望提高靶向治療的針對性和有效性。




 魯ICP備2022037090號
魯ICP備2022037090號
